कोवोवैक्स, कोर्बेवैक्स और एंटी कोविड पिल मोलनुपीराविर के आपात उपयोग की सिफारिश
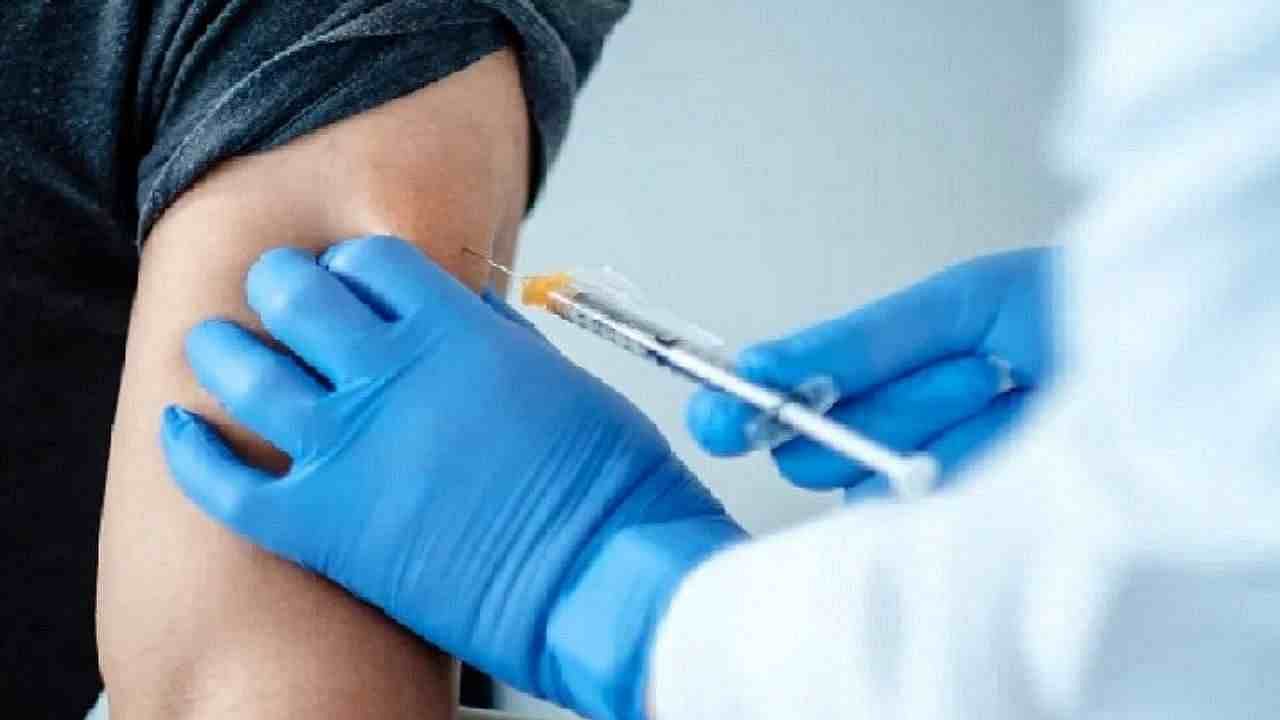
नई दिल्ली. देश के केन्द्रीय औषधि प्राधिकरण (central drug authority) की एक विशेषज्ञ समिति ने सीरम इंस्टीट्यूट ऑफ इंडिया (Serum Institute of India) के कोविड टीके कोवोवैक्स (covovax) और बायोलॉजिकल ई कंपनी के टीके कोर्बेवैक्स (Biological E Co. Corbevax) को कुछ शर्तों के साथ आपात स्थिति में उपयोग की अनुमति देने की सिफारिश की है. आधिकारिक सूत्रों ने बताया कि केन्द्रीय औषधि मानक नियंत्रण संगठन (CDSCO) की कोविड-19 पर विषय विशेषज्ञ समिति (SEC) ने सोमवार को देश में कोविड की दवा मोलनुपीराविर (covid drug molanupiravir) की आपात स्थिति में नियंत्रित उपयोग की सिफारिश की. आपात स्थिति में दवा का उपयोग कोविड-19 के वयस्क मरीजों पर ‘एसपीओ2’ 93 प्रतिशत के साथ किया जा सकेगा और उन मरीजों को यह दवा दी जा सकेगी जिनको बीमारी से बहुत ज्यादा खतरा हो.
सभी सिफारिशों को अंतिम मंजूरी के लिए भारत के औषधि महानियंत्रक (DCGI) के पास भेजा गया है. आपात स्थिति में टीके के उपयोग की सीरम इंस्टीट्यूट ऑफ इंडिया (SII) के आवेदन की सोमवार को दूसरी बार समीक्षा करने वाली CDSCO की विशेषज्ञ समिति ने गहन अध्ययन के बाद कोवोवैक्स के उपयोग की सिफारिश की. एसआईआई में सरकार और नियामक मामलों के निदेशक प्रकाश कुमार सिंह ने इसके संबंध में पहला आवेदन अक्टूबर में दिया था.
Covovax वैक्सीन नोवावैक्स से टेक्नॉलॉजी ट्रांसफर के तहत बनाई गई
एक आधिकारिक सूत्र ने कहा ‘समिति ने पाया किया कि Covovax वैक्सीन नोवावैक्स से टेक्नॉलॉजी ट्रांसफर के तहत बनाई गई है और कंडीशनल मार्केटिंग ऑथराइजेशन के लिए यूरोपीय मेडिसिन एजेंसी द्वारा स्वीकृत है. साथ ही डब्ल्यूएचओ द्वारा आपातकालीन उपयोग में भी लिस्टेड है.’ SII में सरकार और नियामक मामलों के निदेशक प्रकाश कुमार सिंह ने आपात स्थितियों में प्रतिबंधित उपयोग के लिए कोवोवैक्स के लिए बाजार प्राधिकरण प्रदान करने के लिए अक्टूबर में डीसीजीआई में आवेदन किया था.
DCGI कार्यालय ने 17 मई को SII को Covovax के निर्माण और स्टॉक की अनुमति दी थी. DCGI की मंजूरी के आधार पर फर्म ने अब तक वैक्सीन की खुराक का निर्माण और स्टॉक किया है.
कॉर्बेवैक्स और एंटी-कोविड गोली मोलनुपिरवीर की भी सिफारिश
बायोलॉजिकल ई के कॉर्बेवैक्स की बात करें तो 10 दिसंबर को हुई एसईसी की बैठक की सिफारिशों के मद्देनजर फर्म नेफेज 2 के अपडेटेड इंटरिम सेफ्टी और इम्यूनोजेनेसिटी डेटा के साथ वयस्कों के लिए आपातकालीन उपयोग का प्रस्ताव प्रस्तुत किया. कंपनी ने अपने आवेदन में फेज 2 /3 क्लनिकल ट्रायल और फेज 3 एक्टिव कम्परटर ट्रायल का इंटरिम सेफ्टी और इम्यनोजनिसिटी डेटा भी दिया था.
इसके साथ ही SEC ने सोमवार को एसपीओ2′ 93 प्रतिशत के साथ वयस्क COVID-19 रोगियों के इलाज में प्रतिबंधित आपातकालीन उपयोग के लिए एंटी-कोविड गोली मोलनुपिरवीर की मैन्युफैक्चरिंग और मार्केटिंग की अनुमति देने की भी सिफारिश की. सिप्ला, माइलान, टोरेंट, एमक्योर और सन फार्मा के कंसोर्टियम में डॉ रेड्डीज लैबोरेट्रीज ने विभिन्न सहायक दस्तावेजों और क्लिनिकल ट्रायल के डेटा के साथ आपातकालीन स्थिति में अनुमोदन के लिए मोलनुपिराविर 200mg कैप्सूल के अनुमोदन के लिए अपना प्रस्ताव प्रस्तुत दिया था.






